Primer Design. PCR을 통해 특정서열을 증폭해내고자 할때, 원하는 서열을 콕 집어내려면, 서열을 보고 적절한 primer를 디자인해야한다.
약 18-24mer의 oligomer서열과 Tm값을 계산해낼 수 있다. annealing온도의 몇도차이가, 현저한 PCR결과를 만들어낸다.
20base이내인 primer의 Tm값은 다음공식으로 계산될 수 있다.
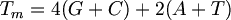
그 이상의 길이에 대해서는 NearestNeighobr계산이 필요하다.
Primer내에 적당한 GC contents가 필요하다. 이 GC함량과 Tm과 값을 잘 맞추어야한다.
PCR 생성물의 길이는 PCR 증폭시 그 효율성에 상당히 영향을 준다. 생성물의 길이는 그 목적에 따라 달라지는데, 특정 부위를 확인하는 목적이라면 120-300 bp가 적당하다.
관련정보
관련프로그램
PrimerDesigner.py : Primer3을 이용한 스크립트
Primer design시 고려되어야 하는 사항
Primer의 3’ terminal sequence
- 5’ terminal sequence는 annealing에 그다지 중요한 역할을 하지 않지만 3’ terminal sequence는 PCR product가 extension하는 부위이기 때문에 PCR의 sensitivity와 specificity에 중요한 역할을 한다. 3개 이상의 G or C은 비특이적인 중폭을 야기하기 때문에 피하는 것이 좋다.
- 또한 3’ terminal에 thymidine이 위치하는 것 역시 피하는 것이 좋다. 왜냐하면 thymidine은 올바르지 못한 다른 염기와의 mispairing 가능성이 높기 때문이다.
- primer-primer dimer를 형성 가능성이 있기 때문에 서로 다른 primer의 3’ terminal sequence간 complementarity 가능성도 고려해야 한다.
- PCR을 통해 site-direct mutagenesis를 유도하는 경우 primer내에 template과 mismatch되는 base가 삽입되어 있으므로 template과의 결합력이 떨어진다. 그러므로 3’ terminal sequence에 template과 match되는 부분이 적어도 3개 이상 나열되게끔 primer를 design해야 한다.
- Primer내에 restriction enzyme recognition site를 삽입하는 경우 5’ terminal sequence를 이용하는 것이 좋다.
Primer의 secondary structure 형성
- Primer내 self-complementary sequence가 있는지 확인하여 secondary structure를 형성 가능성을 배제하여야 한다. Hairpin과 같은 secondary structure를 형성하게 되면 PCR에 치명적인 영향을 줄 수도 있다.
Primer length
- 일반적인 경우 primer size는 18-30mer 가량이 적당하다. Primer 길이가 짧은 경우에는 target sequence외에도 결합할 확률이 높아지기 때문에 specificity가 낮아져 비특이적 증폭이 일어날 수 있다. 하지만 complexity가 낮은 plasmid DNA와 같은 경우에는 다소 짧은 primer도 이용 가능하다
GC content
- 40-60% 로 sense와 antisene primer의 GC content가 비슷하도록 design한다.
Tm and annealing temperature
- Tm: Tm = 2°C x (A+T) + 4°C x (C+G) 로 계산되며 sense와 antisense의 Tm값이 비슷해야 한다.
- 때로는 Tm value는 (H /S+R*ln(C/4))*273 + 16.6 logM 로 표현되기도 한다. 이는 nearest-neighbor방법(PNAS 83, 3746-50)으로 구한 결과이며. GC값을 이용한 방법보다 정확한 것으로 알려져 있다. 여기서 C는 반응에 들어가는 올리고의 농도, M은 반응조건의 salt농도를 말한다.
- annealing temperature는 일반적으로 Tm보다 5도 가량 낮추어 시행하는 것이 좋다.
Primer concentration
- primer의 농도는 0.1-0.5mM 가량이 적당하다. Primer의 농도가 너무 높으면 비특이적인 증폭이 발생하게 된다.
Primer deduced from amino acid sequence
- 정확한 nucleotide sequence를 모르는 상태에서 amino acid sequence로부터 추론하여 DNA을 증폭하고자 하는 경우에는 PCR 조건을 잡기가 매우 까다롭다. 이러한 경우에는 서로 다른 경우의 수에서 비롯된 다양한 primer mixture를 쓰기도 한다. 즉, primer와 template간의 Tm값이 서로 다르기 때문에 Tm값을 조절하면서 PCR 조건을 잡는다.
- 정확한 template sequence를 모르는 상태에서 primer를 design하였으므로 mismatch의 가능성이 높아지게 된다. 이러한 가능성을 줄이기 위해 다양한 codon usage를 가지는 Leu, Arg, Ser(6개 codon usage)보다는 1개 또는 소수의 해당 codon을 가지는 Met, Trp으로부터 유추된 sequence를 3’ terminal sequence에 위치하도록 design한다.
Choice of primer location
- RT-PCR의 경우 Reverse Transcription을 통해 만들어진 cDNA template로부터 PCR를 시행하게 되는데 이때 genomic DNA가 contamination되어 있으면 만들어진 product가 cDNA로부터 증폭된 것인지 genomic DNA로부터 증폭된 것이 판가름하기 힘들어진다. 이 때 PCR에 사용되는 primer의 위치를 exon과 exon 사이로 두게 되면 exon사이에 intron이 위치한 genomic DNA의 경우 결합력이 저하되어 증폭되지 않는다.
Primer for RT-PCR
- cDNA 합성시 사용되는 primer는 크게 세 종류가 있다. 첫째, poly(A) signal에 결합하여 cDNA을 합성시키는 oligo d(T): 둘째, random한 6개 염기로 이루어져 있는 random hexamer, 셋째, gene-specific primer이다.
- Oligo d(T)의 경우 모든 mRNA을 다 cDNA로 바꿔준다.
- Random hexamer의 경우 mRNA, rRNA 등 모든 종류의 RNA를 cDNA로 바꾼다.
- Gene specific primer의 경우, 원하고자 하는 gene of interest의 cDNA만을 형성한다.
궁금함중 한가지. mRNA의 5'UTR영역이 Gene specific하기에, 그부분으로 파악되는 부분으로 PrimerDesign을 하면 좋다고~~~ 왜, 5'UTR영역이 Gene specific한가? 이거, 분자생물학책에 나오는건데 내가 모르고 있는건가? AnswerMe~~ --yong27/2004-08
 BioHackersNet
BioHackersNet